肺癌单细胞文献阅读2
文献
Single-cell transcriptomic analyses provide insights into the cellular origins and drivers of brain metastasis from lung adenocarcinoma
IF:15.9 中科院分区:1区 医学WOS 分区:Q1
背景
脑转移是最常见的恶性颅内肿瘤,约30%的实体瘤会发生,但以肺癌发生率最高。肺癌发生率高,治疗手段有限,且预后差。目前,肺癌脑转移的发生机制暂不明确,因此早期识别BM高危患者十分有必要。
摘要
文章数据:11 LUAD primary tumor (PT) ,10 BM samples (GSE131907)
采用拷贝数变异(CNV)和克隆性分析来说明BM肿瘤的细胞起源。通过伪时间轨迹分析鉴定脑转移相关上皮细胞(BMAEC)。通过使用机器学习算法,开发了BM指数,该指数代表了bulk - RNA-seq数据中BMAECs的相对丰度,揭示BM高风险。基于癌细胞系药物敏感性数据来预测BMAEC的靶向药物。
材料与方法
数据来源:单细胞病人入组选了做手术但未进行用药的病人。TCGA还能通过The Cancer Proteome Atlas获取对应的蛋白质组数据。此外,作者还用了自己的数据(北大协和医学院的)。人类癌细胞系的基因表达谱来自癌细胞系百科全书,癌细胞系的药敏数据来自(CTRP)和PRISM repurposing dataset 19Q4。
结果
1.BM、PT样本间的不同细胞组分和免疫微环境
tsne将样本分成23个簇,后续再根据差异基因注释成10类。总的来说,免疫细胞在两类样本中占大头(图1B与1C),免疫细胞中占比最多的为T细胞。BM中相对PT占比较多的为转移性ECs,其次为T细胞,巨噬细胞(图1D、1E)。二者细胞组分不一致(1F)。
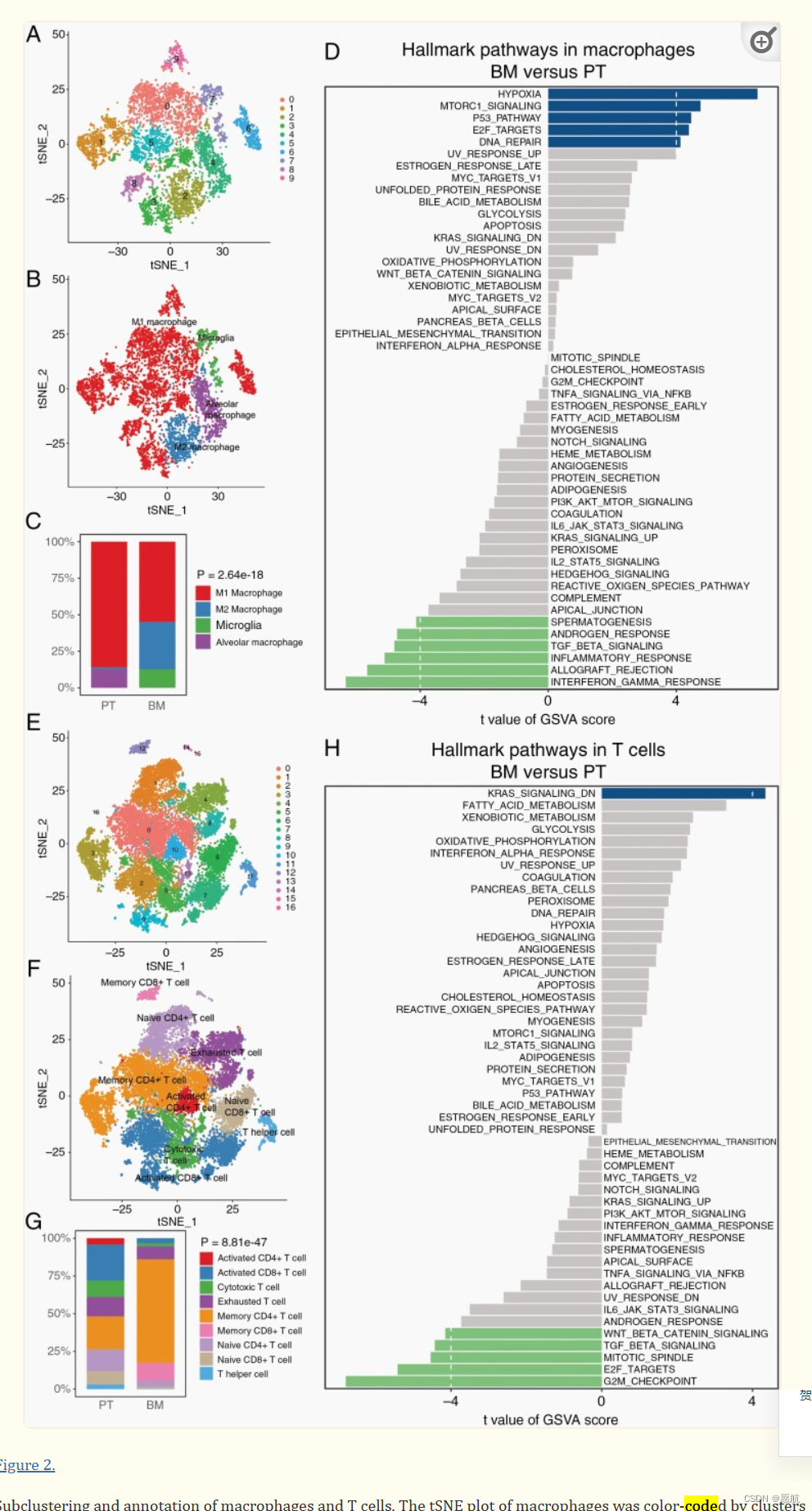
将巨噬细胞重新进行聚类,分成4类(图2A与BB)。其中M1在两类样本中都很丰富,免疫抑制型M2在BM样本中更丰富(2C),M2的富集差异结果在另一数据集得到验证。使用GSVA分析得知,hypoxia, mTORC1 signaling, P53 signaling, and DNA repair被激活在BM巨噬细胞中,而interferon-gamma response, inflammatory response, and TGF-beta signaling pathway则是在PT样本中显著富集(2D)。
将T细胞进行重新聚类,分成9亚型(2E\2F),两类型样本的T组成不同,发现了PT、BM中大部分为CD4+细胞。BM样本中KRAS信号通路被激活,而PT样本中G2/M checkpoint、TGF-beta signaling、Wnt/beta-catenin signaling pathways被激活。

2.CNV和克隆分析揭示BM肿瘤的细胞来源
inferCNV用来分析PT与BM样本的上皮细胞的CNV和克隆性(3a\3b)。在PT样本中的2346个ECs中,1517个有cnv高得分,因此考虑为恶性,819个与参考聚在一块,被认为非恶性(3c)。因为脑组织中没有ec,所以脑内所有ec细胞都为恶性,且脑内的ec细胞cnv分数低的也少。利用进化系统发生树展示肿瘤克隆性和恶性肿瘤细胞的进化,结果为:在PT,所有恶性EC都存在1q扩增,42%的细胞有7p和7扩增。在BM,所有恶性EC都能观察到7p和7q扩增(图3F)。此外,位于7号染色体上的36个基因的拷贝数扩增也被PT中有7p或7q扩增的6个亚克隆细胞亚群共享(3G)。研究还发现位于PT 7号染色体上的100个基因的拷贝数扩增也存在于BM 7p或7q扩增的亚克隆中(3H)。当LUAD转移到脑时,7号染色体上35个基因的拷贝数扩增保持不变,BM样本额外产生65个基因扩增(3I)。
为进一步评估PT和BM样本的瘤内异质性,基于恶性细胞转录组学特征计算每个样本的多样性评分,结果发现PT的多样性评分显著高于BM(3J),而PT中恶性细胞的比例显著低于BM (3 k)。GSVA发现MYC targets, PI3K/Akt/mTOR signaling, epithelial-mesenchymal transition, and cellular metabolism-related pathways路在BM的恶性细胞中显著激活(3L)。

3.伪时序轨迹识别与BM相关的特定EC亚群
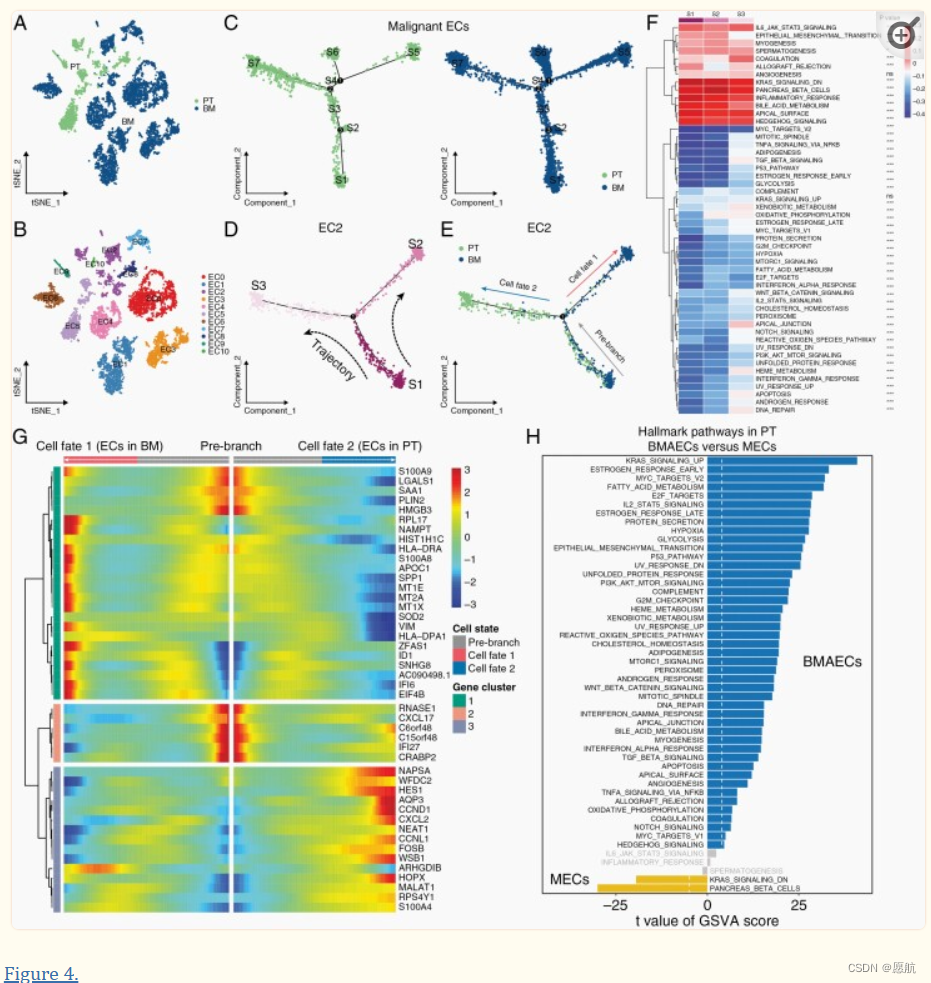
将两类样本的恶性EC细胞聚类,分成11亚群,然后运用拟时序分析。结果观察到来自PT和BM的ECs基本上遵循相似的分化轨迹,并参与了7种细胞状态的转换过程(4C)。在这些细胞亚群中,只有EC2由来自PT和BM样本的细胞组成。因此,进一步对EC2进行了伪时序分析,得到了由细胞命运决定的三个细胞状态(4D),其中状态S2主要富集于BM细胞,状态S3主要富集于PT细胞,状态S1在PT和BM中均富集(4E)。GSVA发现在三种细胞状态中分子通路的激活高度不同(4F)。随后,进行分支表达分析模型(BEAM)分析来确定这三种状态下的分支依赖性基因,总共识别了45个基因,它们可以调节从状态S1(前分支)到S2(细胞命运1)和S3(细胞命运2)的细胞分化过程(4G)。此外,由于EC2经历了从祖细胞到两种不同命运细胞的转换,因此EC2细胞被定义为BMAECs。GSVA分析发现大多数癌症相关通路在BMAECs中被激活(4H)。
4.验证BMAECs与预后转移相关
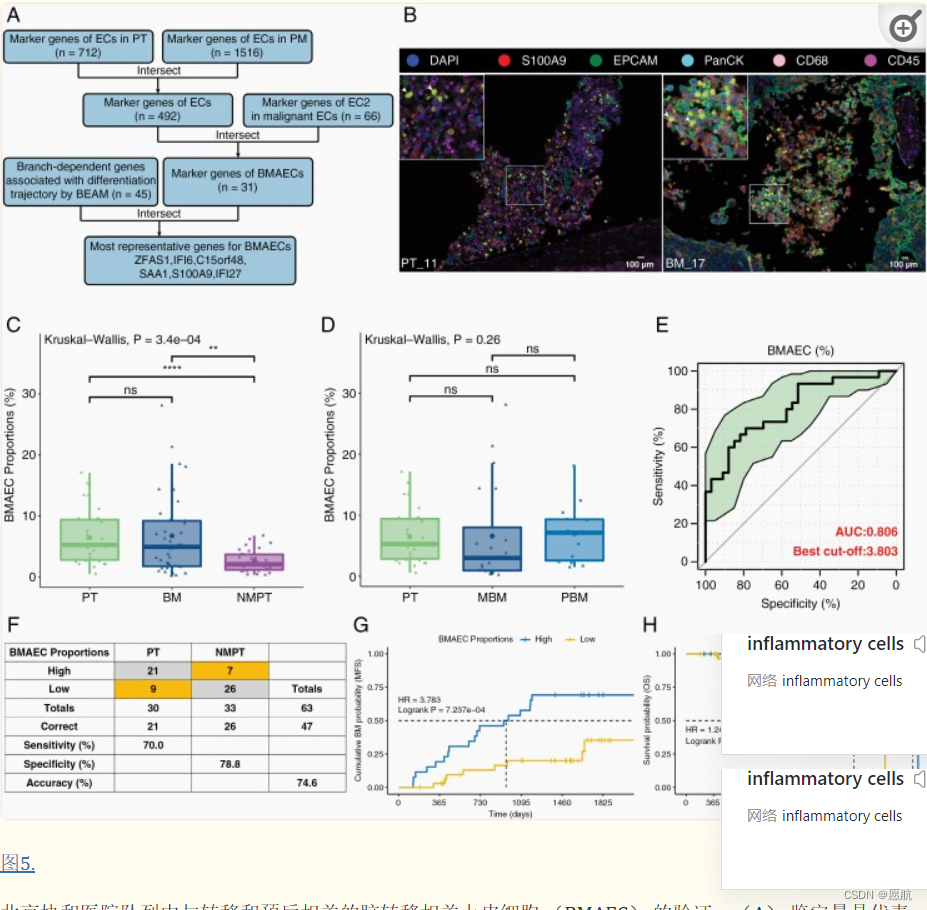
首先识别了ECs和EC2的标记基因,接着取交集作为BMAECs的标记基因。然后,将BMAECs的31个标记基因与跨细胞状态的45个分支依赖基因取交集,并将交集的6个基因定义为BMAECs最具代表性的基因(5A),并选择S100A9作为BMAECs的标志物,结果研究使用标志物有效区分了PT和BM中的S100A9+EPCAM+恶性细胞和S100A9+炎性细胞(图5B)。接下来研究通过ROC分析观察到BMAEC比例在识别LUAD PT脑转移和NMPT方面具有良好的性能(图5E,F)。此外,生存分析显示BMAEC比例高的LUAD患者MFS显著较差(图5 G),而OS无显著差异(图5H)。最后得出结论:BMAEC 在未来脑转移的 LUAD PT 样本中具有明显更高的丰度,并且 BMAEC 的比例越高,患者发生脑转移的时间越早。
5.TCGA-LUAD 队列中 BM 指数与临床病理特征之间的关联
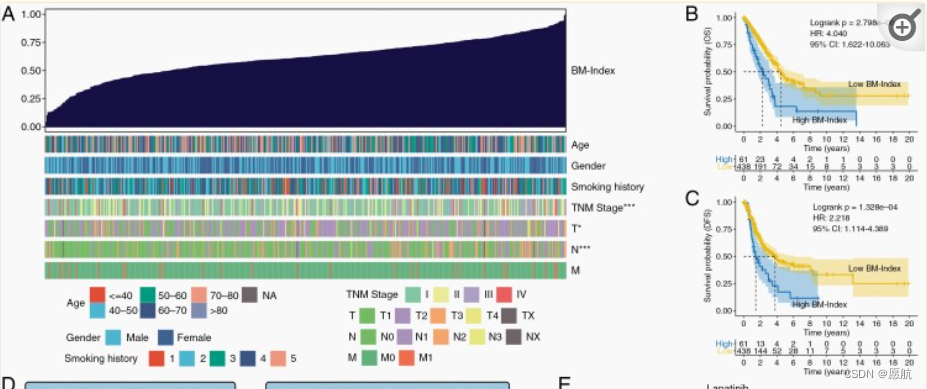
采用logistic回归算法,计算499例TCGA-LUAD患者体积RNA-seq数据的BM指数,以表示BMAECs的相对丰度(图6A).从TNM I期到IV期,BM指数显著升高(P=4.1×10?07),但 T1 显著低于 T2-4 (P = .015),N0 显著低于 N1-3 (P = 4.4 × 10?07) 。单因素和随后的多因素Cox回归分析表明,BM指数是TCGA-LUAD队列中OS和DFS的独立预后预测因子(补充图6B-E)。K-M 生存分析表明,BM 指数高的患者表现出明显更差的 OS(图6B) 和 DFS(图6C).这些发现表明,BMAECs丰度较高的LUAD患者具有较高的TNM分期和较差的预后。
6.针对高BM指数患者的BMAEC治疗药物的鉴定
采用两种不同的方法来识别可以抑制LUAD脑转移的候选药物,包括靶向BMAEC的高度敏感药物和高BM指数(图6D).我们获得了 78 种用于靶向 BMAEC 的 CTRP 化合物和 65 种 PRISM 化合物,以及 23 种用于高 BM 指数患者的 CTRP 化合物和 171 种 PRISM 化合物。通过做交集,最终确定 2 种 CTRP 药物(拉帕替尼和西比林)和 5 种 PRISM 药物(LGX818、repsox、RG2833、辛伐他汀和托司他)为治疗脑转移的候选药物,其 BMAEC 和高 BM 指数患者的 AUC 值显着降低,并与 BM 指数呈负相关(图6E和补充图7)。拉帕替尼是研究其对肺癌脑转移的抑制的首选。考虑到拉帕替尼的药物靶点mRNA水平,EGFR、ERBB2和RIPK2在BMAECs中与MECs相比,与AUCs呈高表达且呈负相关(图6F).同样,ERBB3、PIK3C2B、EGFR和ERBB2在高BM指数患者中高表达,与AUCs呈负相关(图6G).考虑到药物靶点的蛋白水平,EGFR和EGFR-pY1068在高BM指数患者中高表达,与AUCs呈负相关(图6H).因此,EGFR被确定为拉帕替尼治疗LUAD脑转移的潜在靶点。需要进一步的研究来验证这些药物通过靶向 BMAEC 和高 BM 指数患者抑制 LUAD 脑转移的治疗价值。
讨论
1.尽管我们发现LUAD和BM之间的免疫微环境存在差异,但需要进一步的研究来确认免疫细胞是否对LUAD脑转移有影响
2.BM及其潜在标志物S100A9的细胞来源在我们的研究中通过scRNA-seq数据确定。然而,S100A9通常被认为是炎症细胞(如中性粒细胞或单核细胞)的标志物。尽管我们已经通过多重IF证实了EPCAM和S100A9的共定位,但明确区分S100A9阳性肿瘤细胞和炎症细胞可能具有挑战性。
本文来自互联网用户投稿,该文观点仅代表作者本人,不代表本站立场。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。 如若内容造成侵权/违法违规/事实不符,请联系我的编程经验分享网邮箱:chenni525@qq.com进行投诉反馈,一经查实,立即删除!