基于3D-CGAN的跨模态MR脑肿瘤分割图像合成
3D CGAN BASED CROSS-MODALITY MR IMAGE SYNTHESIS FOR BRAIN TUMOR SEGMENTATION
基于3D-CGAN的跨模态MR脑肿瘤分割图像合成
2018 IEEE 15th International Symposium on Biomedical Imaging (ISBI 2018)
背景
脑肿瘤的分割需要多种模态影像的共同作用。不同模态的影像可以从不同角度表示肿瘤的组织变化,将它们协同考虑有利于脑肿瘤的分割。同时,考虑到获取多模态图像的成本,研究从T1合成Flair图像是否有助于从T1的单一模态改进脑肿瘤分割,通过设计用于Flair图像合成的3D cGan和局部自适应融合,更好地描述合成Flair图像的细节。这种方法可以有效地处理不同样本在外观、大小和位置上不同的脑肿瘤的分割任务。
贡献
- 由于现有的2D cGan引起的跨切片不连续问题,提出3D cGan,通过考虑上下文信息更好地合成Flair图像。
- 为了进一步改进合成的Flair图像用于分割任务,提出一种局部自适应合成方法,更好地描述合成的Flair图像的局部细节。
- 通过训练联合考虑多种成像的CNN,利用合成的Flair图像来辅助从单个T1模态进行脑肿瘤分割
实验
3DcGan + 局部自适应融合,合成的图像+T1图像通过双通道3D CNN分割模型进行处理,分割脑肿瘤
最终目标,合成Flair图像以提高脑肿瘤的分割精度,与那些专注于提高PSNR的合成方法相比,对输出图像的质量提出了更高的要求。
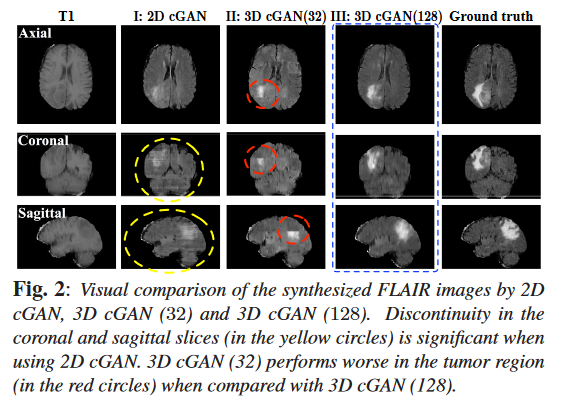
冠状面、矢状面的伪影表示在3D切片上合成效果不连续
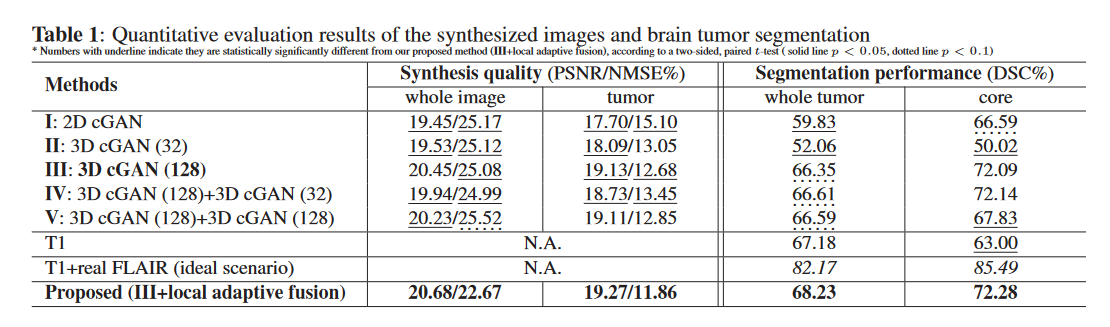
IV、V表示使用级联的3D cGan无法进一步提升效果,但3D cGan整体精度优于2D cGan
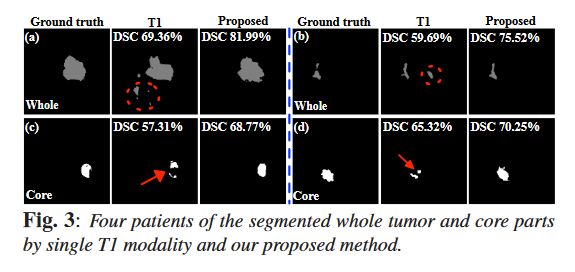
方法
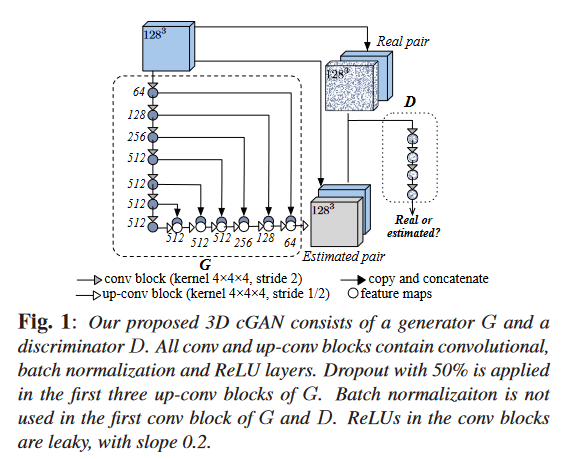
Subject-specific local adaptive fusion(针对特定主题的局部自适应融合)
对于仅具有T1-MR图像的测试对象,我们将其类FLAIR图像从我们的3D c-GAN划分为不重叠的小块(16x16x16),并通过训练块Str,GAN 1,Str,gan2…的凸组合来近似每个块Ste,GAN。。。,Str、gan、Ntr(Ntr表示训练对象的数量)。这是通过解决以下优化问题来实现的:
人话:把原始影像分成16x16x16的patch给每个patch分配不同的权重
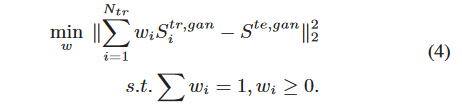
线性组合比局部非线性映射给出更好的结果。尽管这种凸组合会产生一些影响合成图像外观的伪影,但它被证明是改进分割的有效策略,而分割是我们的最终目标。
Brain tumor segmentation model
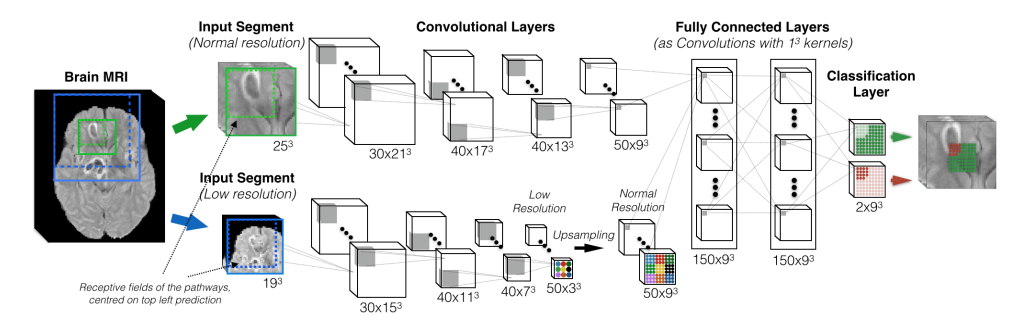
使用这篇论文的框架 [Efficient multi-scale 3d cnn with fully connected crf for accurate brain lesion segmentation],上述分割模型采用两个输入通道:T1和FLAIR。我们分两步训练模型。在第一步中,训练样本的T1和真实FLAIR图像以正常的方式用于训练。然后,在第二步中,使用T1和我们合成的训练样本的FLAIR图像进一步微调该模型。微调是至关重要的,因为对于给定的测试样本,用于分割的是合成的FLAIR图像,而不是真实的未知FLAIR图像。
损失函数
Thinking
3D cGan训练合成网络,先训练T1合成Flair,再利用T1和Flair进行分割,测试时只需要输入T1数据,无Flair数据。
本文来自互联网用户投稿,该文观点仅代表作者本人,不代表本站立场。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。 如若内容造成侵权/违法违规/事实不符,请联系我的编程经验分享网邮箱:chenni525@qq.com进行投诉反馈,一经查实,立即删除!
- Python教程
- 深入理解 MySQL 中的 HAVING 关键字和聚合函数
- Qt之QChar编码(1)
- MyBatis入门基础篇
- 用Python脚本实现FFmpeg批量转换
- CC工具箱使用指南:【要素类追加至空库(批量)】
- 数据采集卡:USB2.0总线,4通道同步、24位156KHz AD,16路DIO
- PostgreSQL 获取指定根节点及其所有子集的id
- lumen自定义封装api限流中间件
- TSKE 系列液氮低温恒温器
- 鸿鹄电子招投标系统源码实现与立项流程:基于Spring Boot、Mybatis、Redis和Layui的企业电子招采平台
- FileStream文件操作
- 【工具篇】Jetson Xavier NX环境搭建
- 掌握 Babel:让你的 JavaScript 与时俱进(上)
- 时间序列(Time-Series)exp_imputation.py代码解析