阅读文献-胃癌
写在前面
今天先不阅读肺癌的了,先读一篇胃癌的文章
文献
An individualized stemness-related signature to predict
prognosis and immunotherapy responses for gastric cancer
using single-cell and bulk tissue transcriptomes
IF:4.0 中科院分区:2区 医学WOS 分区:Q2
亮点:不像其他生信文章,用什么lasso、svm,然后基于表达值做风险得分,而是基于基因间的秩次关系,从而克服了批次效应。
可以学习的点
1.from the Tumor Immune Single Cell Hub 2 database (http://tisch.
comp-genomics.org/), were annotated into malignant
cells, stromal cells, and immune cells.
tisch的使用教程:https://www.cn-healthcare.com/articlewm/20230530/content-1557644.html
这个到底是怎么回事
2.CytoTRACE score如何计算,为细胞干性得分,评估单细胞数据中各细胞亚群的分化潜力,从而鉴定出祖细胞。
3.aucells,定义出的基因集的aucells。
4.为什么GSE134520,分出3组,要找恶性相对于其他两类上调的基因。
所有的基因集得分有没有可能是最后鉴定出的167个跟干细胞相关的基因。
结果
1.鉴定stemness-related signature genes
1)we calculated CytoTRACE scores of malignant cells to estimate their stemness
2)579 genes showed positive correlation with the stemness scores were set as G1 (Pearson R?>?0.2 and FDR <0.05), and genes upregulated in malignant cells were set as G2. The 175 overlapping genes between G1 and G2 were defined as stemness-related signature genes。
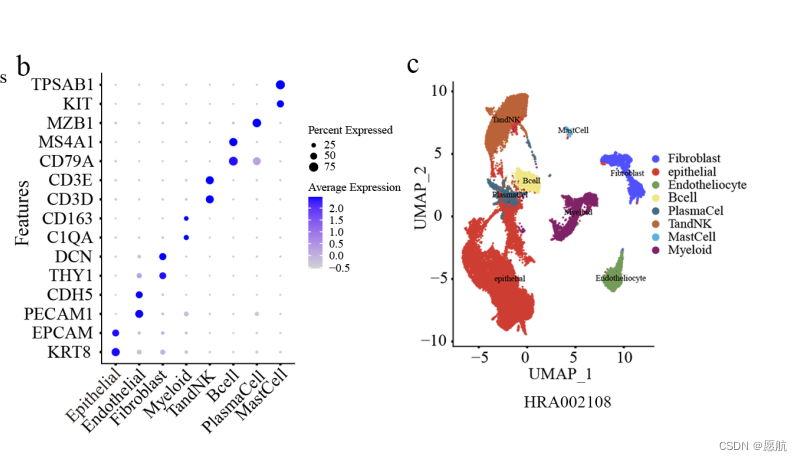
3)在额外的数据集验证,这边想问下是怎么验证的?应该是有背景知识在的,b图应该指的是找到的基因集能特异识别出某细胞类型。
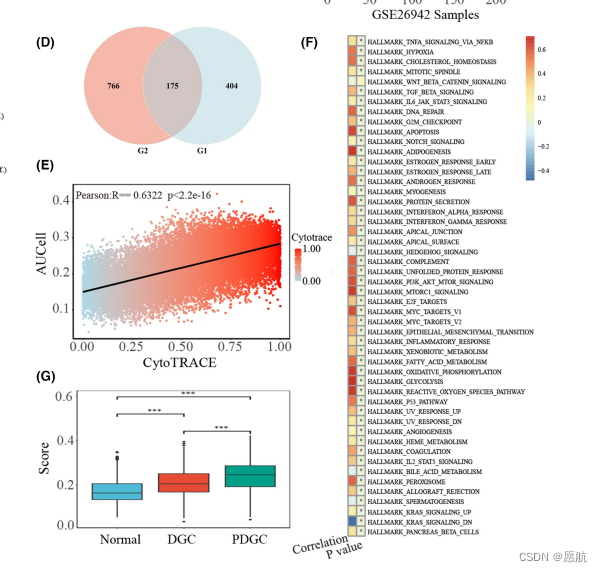
4)也是一个额外的验证。数据基于定义的基因集算出的aucell得分与未基于基因集算出的cytotrace得分,正相关,侧面说明定义的该基因集与细胞干性的相关性。不过我觉得这个aucell得分可能也与G1基因集的定义有关。
2.将GC样本进行分组
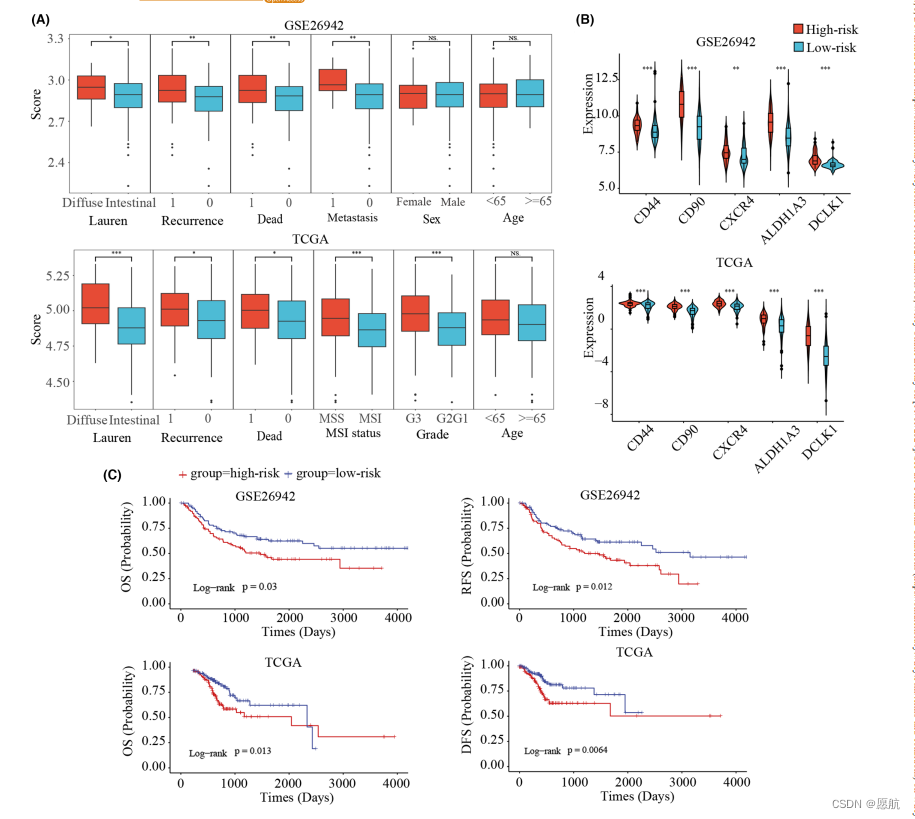
基于基因集做ssgsea打分,算不同临床分组的打分情况,发现符合真实世界,而后再看不同ssgsea打分组的生存差异,上述结果都不错。
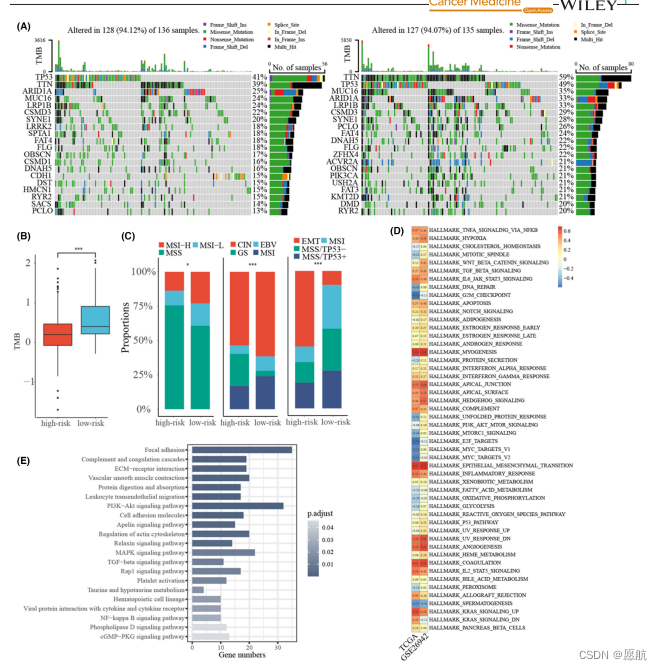
3.看分组的基因组特征与分子特征
看突变情况与MSI、TMB、同路。
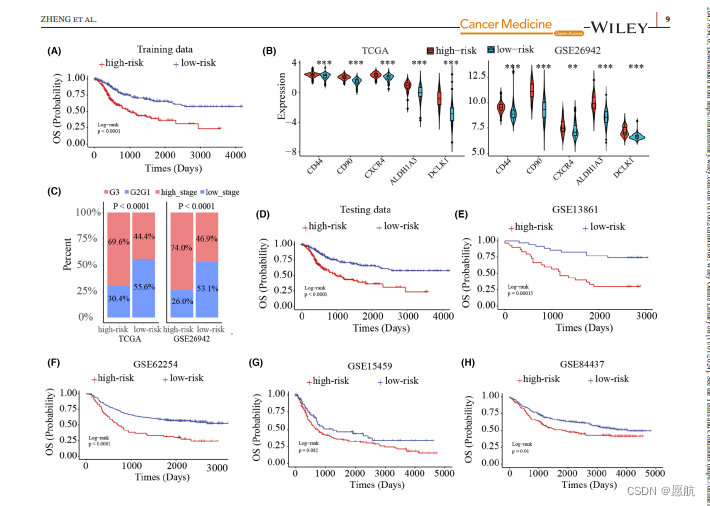
4.开发REO模型与验证
基于秩次关系与半数投票,构建后观察分组表现,及不同临床分组的模型结果比例。额外4套数据再验证,算是比较多的了。
5.看GPS与免疫治疗的关系
1)estimate看基质细胞、肿瘤、M2巨噬细胞,高风险组M2高,目前高M2风险组预后差,又是一个验证。
2)tide网站看高风险组的免疫治疗抗性高,可能不敏感。
3)submap 预测能否对PD-1响应,高风险组不响应,一个验证。
本文来自互联网用户投稿,该文观点仅代表作者本人,不代表本站立场。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。 如若内容造成侵权/违法违规/事实不符,请联系我的编程经验分享网邮箱:chenni525@qq.com进行投诉反馈,一经查实,立即删除!
- Python教程
- 深入理解 MySQL 中的 HAVING 关键字和聚合函数
- Qt之QChar编码(1)
- MyBatis入门基础篇
- 用Python脚本实现FFmpeg批量转换
- Linux之基础I/O
- 德祥堂:遵循中医理论下的“药食同源”之路
- flutter file_picker dio web端上传记录
- 老用户可买:腾讯云轻量应用服务器2核2G4M带宽118元一年,3年540元
- 基础算法(6):前缀和
- “华为杯”研究生数学建模竞赛2016年-【华为杯】B题:具有遗传性疾病和性状的遗传位点分析(附R语言和Python代码实现)
- 微信小程序开发系列-02注册小程序
- 编写一个简单的服务和客户端(C++)
- Linux文本处理指令cut-man帮助手册
- ESLint格式化程序消失,怎么解决